加入收藏
文字:[ 大 中 小 ]
报告简介
随全球药品市场竞争日益激烈,制药产业链中的分工日趋显著,医药企业呈现出将自身研发与生产业务委托给其他专业化公司开展的大趋势。其由于研究内容的专业化程度的强化,资源的有效整合与融合,促进了从疾病目标研究、药物化合物的筛选和研发、临床试验,到规模化工艺优化、委托生产加工乃至市场销售的全产业链各环节的健康发展,涌现出众多的外包服务机构――“让专业的人,做专业的事”。推进了新药物、医械的诞生与市场化的发展,使人类受益。
CRO行业概述
医药研发外包,简称CRO,是一个新兴的专属性的科研服务性行业,其是承接生物医药创新型药物研究过程中某一部分专业性较强的,且又能与研究整体融合互补的工作。其最早起源单纯的药理、毒理的委托,再由此发展成活性物质筛选、化学合成工艺等等内容,其服务内容的分类与创新药物注册政策有关密切的关系;各国药修正为应对政策与科技技术的发展,加速药物研发的产出和降低应专业设置的不足所带来的风险,均有效地采用CRO的研发方式。也使得此科研服务性行业(CRO)的有序发展。
随着国内生物医药、创新型医疗器械、AI技术研发热情的日益高涨,创新性生物医药诞生路径也随着技术发展而变得广大,如活性生物小分子、多肽类、靶向性、仿制药一致性评价、智能型医疗器械、NGS、生物信息技术等多方向性的扩展,专业的所属性研究不断强化与发展,加速了生物医疗大门类研究的速率,另外又由于青苗产出的机制与融资方式,更突显出CRO在研发中所体现的价值,CRO的身价也随之水涨船高,一大批本土优秀CRO企业迅速崛起,受到了资本市场的青睐,中国CRO产业也迎来了新的高峰。国内的CRO产业在未来将呈以下发展趋势。
1、CRO公司提供一站式综合服务
CRO外包服务在全球可以涵盖医药研发的整个阶段,国际CRO产业巨头在发展的过程中无一不通过并购与合作,积极拓展核心业务,积极往一站式CRO服务发展。因此从新药研发到新药上市,一般大型跨国CRO企业都能提供一站式综合服务。我国目前CRO整体行业刚刚起步,产业规模发展潜力巨大。对于本土CRO企业来说,未来如何打造完整的产业服务链不仅可以提高我国制药工业的技术创新能力、推动我国尽快进入制药工业价值链的上游,更是为了满足我国医药市场日益增长的需求,是大势所趋的必然结果。
据调查,目前在国内CRO业务纵向一体化趋势明显加速,一些国内CRO企业开始通过投资、并购的方式来拓展产品线及服务。另外随着国内优秀CRO企业上市,大量资金涌入CRO产业,并购整合或将加速,产业集中度将加强。
2、 国内CRO产业竞争加剧
随着中国加入ICH(人用药品注册技术要求国际协调会)之后,国内药品研发、临床试验在准入机制、先进性、规范性、可操作性上将进一步得到加强,国内CRO企业将面临更加严酷的国际竞争与更加严格的国际标准,是机遇也是挑战。临床试验基地产能瓶颈将被突破、临床试验审批流程和执行速度将加快,临床试验CRO订单数量有望实现快速增长,收入确认周期也将缩短,加快业绩释放。
未来随着CRO产业的不断壮大,竞争必然趋向于国际化。本土企业如何有效与跨国企业合作、消化吸收先进技术、形成自己特色的技术优势以适应新的竞争环境将是摆在面前的重要课题。
3、重磅政策或促进医疗器械CRO产业爆发
2017年5月11日至12日,NMPA连发4份征求意见稿。鼓励药品医疗器械创新,征求意见稿包括:《关于鼓励药品医疗器械创新实施药品医疗器械全生命周期管理的相关政策》、《关于鼓励药品医疗器械创新改革临床试验管理的相关政策》、《关于鼓励药品医疗器械创新加快新药医疗器械上市审评审批的相关政策》、《关于鼓励药品医疗器械创新保护创新者权益的相关政策》。此次NMPA的政策组合拳是从药品研发、临床试验、产品所有者权益和生产企业整条产业链的源头进行政策引导、鼓励药品和医疗器械的创新,简化监管流程,提升审批速度。
最初中国的医疗器械企业比较少,因此有大量的国外企业和国内代理商将医疗器械直接进口进行销售,后来演变为在国内建厂。而这一过程中,需要对国内的政策法规进行适应,这也是医疗器械CRO的早期业务。这些企业更倾向于去找一些比较大的CRO企业进行合作,因为其平台大,资金充足,能够比较好的满足企业的需求。
然而随着国内企业的发展,涉及领域日益广泛,门类越发多样,产品日趋专业化,许多大的公司不能提供专业性的指导和服务,因此一些医疗器械企业由于其产品的专业性需要更加专业的配套CRO企业进行服务,这便为一些专业背景很强的新兴企业提供了成长的机会。
医药生产外包服务企业(医药CMO),是以合同定制形式为制药企业提供临床用药、中间体制造、原料药生产、制剂生产以及包装等专业服务的企业。而伴随CMO市场趋于成熟,定制研发生产(CDMO)、产研结合(CRO+CMO/CDMO)等多种商业模式得以快速发展。
CMO/CDMO行业概述
从产业链来看,CDMO处于药物研发至商业化销售的中间关键环节,其上游为临床前研发CRO环节,下游为药品上市后持续的CMO生产环节。由于创新药领域不断发展、研发成本和风险居高不下,越来越多的下游医药制造企业会选择CMO/CDMO服务,以便为医药企业节约成本、控制风险并提升研发效率,可以预见CMO/CDMO市场规模将不断放大。
我国CRO行业呈现出起步晚,发展快,分布集中的特点。进入21世纪后,药明康德、泰格医药等CRO企业的创立,标志着我国CRO行业的正式起步。2003年,凭借NMPA推出的《药物临床试验质量管理规范》,CRO企业迅速成长壮大。2007年,药明康德登陆纳斯达克,2012年,泰格医药登陆创业板。在资本的追逐下,我国CRO行业正式迎来黄金发展期。
在地域分布上,我国CRO企业主要集聚于北京、上海和江苏。在企业规模上,北京拥有昭衍新药和康龙化成等上市公司;昆泰、药明康德、精鼎、美迪西等龙头公司集聚上海;江苏省则集中培育了一大批新兴CRO知名企业,如华威医药、金思瑞等。
在企业规模上,我国医药CRO企业整体规模较小。营业收入低于1千万元的CRO企业占比超过75%。这源于小型CRO公司进入壁垒较低,尤其是随着药品上市许可持有人制度的完善,一大批科研团队投身CRO领域。药明康德作为国内CRO龙头企业,2017年市场份额占比16.4%,远远超过其它竞争者。在未来的一段时间内,我国CRO行业将维持龙头企业带动,中小创企业推动的局面。
高速增长,行业规模跃升。短期来看,通过对标国际CRO行业的发展路径,我国CRO行业将保持高速增长,行业规模逐步提升,核心竞争力进一步加强。尤其是随着国家政策的引导、审评审批的加速、研发投入的加大、创新能力的提升和人才队伍的扩充,CRO行业的渗透率将逐步提升,需求将进一步释放。
强者恒强,行业整合加剧。长期来看,我国CRO行业整体规模的提升,带来行业竞争的加剧。竞争的加剧推动行业内活跃的兼并收购活动。通过兼并收购,CRO企业推动实现原有业务的拓展,增强企业在产业链中的资源整合能力,促进业务纵向一体化、横向全球化的发展。目前,行业内整合已初具规模,如药明康德收购NextCoDE、Crelux,加强精准医疗布局;泰格医药收购方达医药,加强临床前CRO业务等。从目前的趋势看,未来CRO行业集中度将快速提升,药物一体化研发能力趋于成熟,行业洗牌加剧,强者恒强效应凸显。
报告目录
2025-2030年中国生物医药外包(CRO/CMO/CDMO) 产业现状调查及未来趋势研判报告
第一章 2023-2025年国内外生物医药产业发展状况分析
1.1 生物医药产业概述
1.1.1 生物医药定义
1.1.2 生物医药特点
1.1.3 生物医药注册分类
1.2 全球生物医药产业发展现状分析
1.2.1 全球生物医药市场现状
1.2.2 生物医药全球竞争态势
1.2.3 生物医药重点技术风口
1.2.4 市场集中度变化情况
1.2.5 生物医药产业集群发展
1.3 中国生物医药产业发展驱动因素
1.3.1 政策扶持推动产业发展
1.3.2 技术创新引领产业发展
1.3.3 资金流向市场推动发展
1.4 中国生物医药产业发展现状分析
1.4.1 生物医药行业市场规模
1.4.2 生物医药细分市场分析
1.4.3 生物医药产业发展特点
1.4.4 生物技术进口状况分析
1.5 中国生物医药产业未来发展趋势
1.5.1 政策持续规范发展
1.5.2 产业创新态势加速
1.5.3 重点领域发展态势
第二章 2023-2025年中国生物医药外包行业发展逻辑深度分析
2.1 中国生物医药外包自身发展优势
2.1.1 人才优势
2.1.2 资本优势
2.1.3 市场优势
2.1.4 模式优势
2.2 生物医药企业外包意愿上升
2.2.1 专利断崖倒逼药企
2.2.2 医药研发外包意愿高
2.2.3 全球研发管线数量增长
2.3 生物医药企业成本控制意愿增强
2.3.1 研发周期漫长
2.3.2 研发成本猛增
2.3.3 研发回报下降
2.4 中国医药行业政策利好医药外包市场
2.4.1 创新药政策利好接轨全球
2.4.2 新药海外国内上市时间缩短
2.4.3 药品上市许可持有人制度助推
2.4.4 政策市场双驱动成效明显
2.5 中国生物医药融资环境持续向好
2.5.1 中小生物医药企业兴起
2.5.2 生物医药行业融资活跃
第三章 2023-2025年中国生物医药外包市场发展状况分析
3.1 生物医药外包行业关键指标解释
3.1.1 医药合同外包
3.1.2 医药研发外包(CRO)
3.1.3 医药生产外包(CMO)
3.1.4 医药生产研发外包(CDMO)
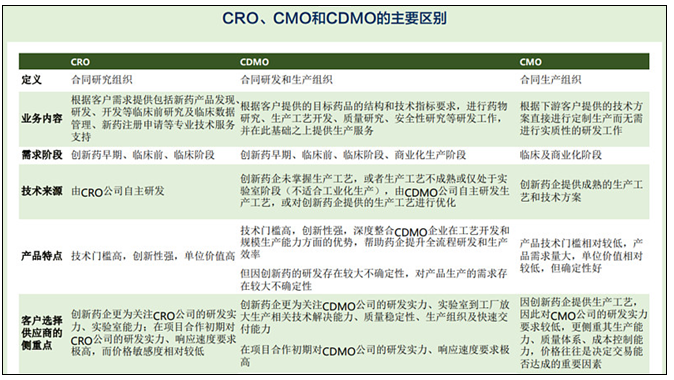
3.1.5 CMO与CDMO异同
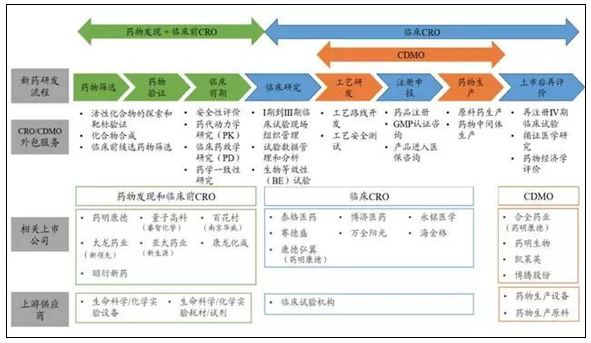
3.1.6 医药外包产业链条
3.2 中国生物医药外包行业发展综述
3.2.1 行业基本概述
3.2.2 行业政策支持
3.2.3 中外模式对比
3.2.4 市场发展规模
3.2.5 产业集群发展
3.3 生物医药外包发展案例深度剖析
3.3.1 产业发展案例
3.3.2 地区发展案例
3.3.3 园区发展案例
3.4 中国生物医药外包市场发展建议
3.4.1 完善人才政策
3.4.2 加大财税扶持
3.4.3 优化行业监管
3.4.4 强化产权保护
第四章 2023-2025年中国生物医药研发外包(CRO)市场分析
4.1 医药研发外包相关概述
4.1.1 医药研发外包业务分类
4.1.2 医药研发外包维度结构
4.1.3 产业上下游关联度分析
4.2 2023-2025年中国生物医药研发外包发展分析
4.2.1 发展历程分析
4.2.2 市场规模分析
4.2.3 区域分布格局
4.2.4 产业服务内容
4.2.5 发展模式分析
4.3 中国生物医药研发外包未来发展趋势
4.3.1 市场集中度提升趋势
4.3.2 产融结合发展趋势
4.3.3 深度介入研发趋势
4.3.4 专业投资发展趋势
第五章 2023-2025年中国生物医药生产外包(CMO)市场分析
5.1 医药生产外包相关概述
5.1.1 医药生产外包特点
5.1.2 医药生产外包企业性质
5.1.3 医药生产外包产业链条
5.2 2023-2025年中国生物医药生产外包发展状况
5.2.1 行业政策利好
5.2.2 行业发展优势
5.2.3 企业经营状况
5.2.4 订单数量分析
5.2.5 产业链拓展情况
5.3 中国生物医药生产外包未来发展前景
5.3.1 市场发展潜力
5.3.2 未来发展方向
5.3.3 行业发展路径
第六章 2023-2025年中国生物医药生产研发外包(CDMO)市场分析
6.1 中国医药生产研发外包服务概述
6.1.1 服务环节
6.1.2 服务内容
6.1.3 订单分类
6.2 2023-2025年中国生物医药生产研发外包发展现状
6.2.1 行业发展历程
6.2.2 行业发展背景
6.2.3 全球市场规模
6.2.4 中国市场规模
6.2.5 企业业务范围
6.2.6 企业竞争优势
6.3 生物医药生产研发外包企业发展壁垒
6.3.1 行业监管壁垒
6.3.2 客户信任壁垒
6.3.3 行业技术壁垒
6.4 生物医药生产研发外包发展趋势分析
6.4.1 精细化分工趋势
6.4.2 一体化研发趋势
第七章 2023-2025年国外医药生物CRO/CMO/CDMO重点企业运营分析
7.1 Charles River Laboratories International, Inc.
7.1.1 企业基本介绍
7.1.2 2023年企业经营状况分析
7.1.3 2024年企业经营状况分析
7.1.4 2025年企业经营状况分析
7.2 Catalent, Inc.
7.2.1 企业基本介绍
7.2.2 2023年企业经营状况分析
7.2.3 2024年企业经营状况分析
7.2.4 2025年企业经营状况分析
7.3 龙沙集团(Lonza Group AG)
7.3.1 企业基本介绍
7.3.2 2023年企业经营状况分析
7.3.3 2024年企业经营状况分析
7.3.4 2025年企业经营状况分析
第八章 2022-2025年中国医药生物CRO/CMO/CDMO标杆企业运行分析
8.1 浙江九洲药业股份有限公司
8.1.1 企业基本介绍
8.1.2 企业最新态势
8.1.3 经营效益分析
8.1.4 业务经营分析
8.1.5 财务状况分析
8.1.6 核心竞争力分析
8.1.7 公司发展战略
8.1.8 未来前景展望
8.2 无锡药明康德新药开发股份有限公司
8.2.1 企业发展概况
8.2.2 经营效益分析
8.2.3 业务经营分析
8.2.4 财务状况分析
8.2.5 核心竞争力分析
8.3 杭州泰格医药科技股份有限公司
8.3.1 企业发展概况
8.3.2 经营效益分析
8.3.3 业务经营分析
8.3.4 财务状况分析
8.3.5 核心竞争力分析
8.3.6 未来前景展望
8.4 重庆博腾制药科技股份有限公司
8.4.1 企业发展概况
8.4.2 经营效益分析
8.4.3 业务经营分析
8.4.4 财务状况分析
8.4.5 核心竞争力分析
8.4.6 公司发展战略
8.4.7 未来前景展望
8.5 上海合全药业股份有限公司
8.5.1 企业发展概况
8.5.2 企业技术优势
8.5.3 经营效益分析
8.5.4 业务经营分析
8.5.5 财务状况分析
8.5.6 核心竞争力分析
8.5.7 公司发展战略
8.5.8 未来前景展望
8.6 凯莱英医药集团(天津)股份有限公司
8.6.1 企业发展概况
8.6.2 经营效益分析
8.6.3 业务经营分析
8.6.4 财务状况分析
8.6.5 核心竞争力分析
8.6.6 公司发展战略
8.6.7 未来前景展望
8.7 上市公司财务比较分析
8.7.1 盈利能力分析
8.7.2 成长能力分析
8.7.3 营运能力分析
8.7.4 偿债能力分析
第九章 2025-2030年生物医药外包行业发展前景及趋势预测
9.1 CRO/CDMO行业一体化趋势剖析
9.1.1 一体化是企业发展必然趋势
9.1.2 符合客户价值延伸趋势要求
9.1.3 企业可实现业务拓展的需要
9.1.4 跟随创新药发展阶段的策略
9.1.5 一体化企业最具市场竞争力
9.2 2025-2030年中国CRO/CMO/CDMO行业预测分析
9.2.1 2025-2030年中国CRO/CMO/CDMO行业影响因素分析
9.2.2 2025-2030年中国CRO市场规模预测
9.2.3 2025-2030年全球CMO/CDMO市场规模预测
9.2.4 2025-2030年中国CMO/CDMO市场规模预测
第十章 CRO/CDMO一体化企业案例分析――药明康德
10.1 药明康德企业发展综述
10.1.1 企业发展历程
10.1.2 企业业务领域
10.1.3 企业治理情况
10.1.4 企业新药研发体系
10.1.5 企业业务收入分析
10.2 药明康德主要业务板块分析
10.2.1 业务单元拆分
10.2.2 中国试验区服务
10.2.3 美国区实验室服务
10.2.4 临床研究及其他CRO服务
10.2.5 小分子新药工艺研发及生产CMO/CDMO业务
10.3 药明康德核心竞争力分析
10.3.1 “一站式”服务优势
10.3.2 企业人才优势
10.3.3 商业模式优势
10.3.4 海外业务优势
10.3.5 “长尾”战略优势
第十一章 CDMO龙头企业案例分析――凯莱英
11.1 凯莱英CDMO业务发展分析
11.1.1 业务发展历程
11.1.2 主营业务范围
11.1.3 同行业务对比
11.1.4 业务详情分析
11.2 凯莱英CDMO业务竞争优势分析
11.2.1 技术领先优势
11.2.2 客户深度合作
11.2.3 产能预备充足
11.2.4 人才储备丰富
11.3 凯莱英CDMO业务订单发展分析
11.3.1 商业化阶段项目
11.3.2 临床阶段项目
11.3.3 技术开发项目
11.4 凯莱英CDMO领域布局情况分析
11.4.1 CRO方面发展布局
11.4.2 大分子CDMO方面
11.4.3 产业基金投资方面
|

