报告简介
Humira为全球最畅销生物药
生物药为药品的子类别。与化学药(化学合成的小分子物质)不同,生物药是源自多种天然来源或通过生物技术方法生产的大分子物质。生物药产品范围广泛,涵盖抗体(例如mAbs、ADCs及BsAbs)、重组蛋白、疫苗及其他新兴类别。
2019年全球生物药销售规模誉为2864亿美元,中国市场销售额为3120亿美元。
中国生物类似药起步较晚
根据主管部门的规定,尽管辅料可能存在细微差别,惟生物类似药通常定义为在质量、安全及疗效方面与已获批准的生物药(即原研药或参照药)高度相似的生物药品。2019年全球生物类似药市场规模为95亿美元,2015-2019年的复合年增长率为37.5%。
2015-2020年全球生物类似药市场规模
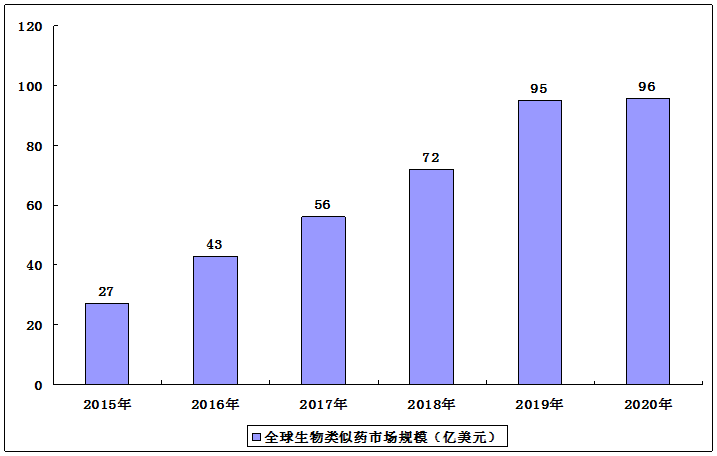
尽管中国生物类似药的监管审批路径在最近《生物类似药研发与评价技术指导原则》发布后才建立,但中国生物类似药市场快速增长,自2019年起获批包括格乐立在内的六个生物类似药。2020年6月,《药品注册管理办法(2020年)》及《生物制品注册分类及申报资料要求》进一步订明中国生物类似药的分类,在日趋清晰的监管体制下塑造中国生物类似药的发展。中国生物类似药市场规模在2019年达到23亿元左右。
2015-2020年中国生物类似药市场规模
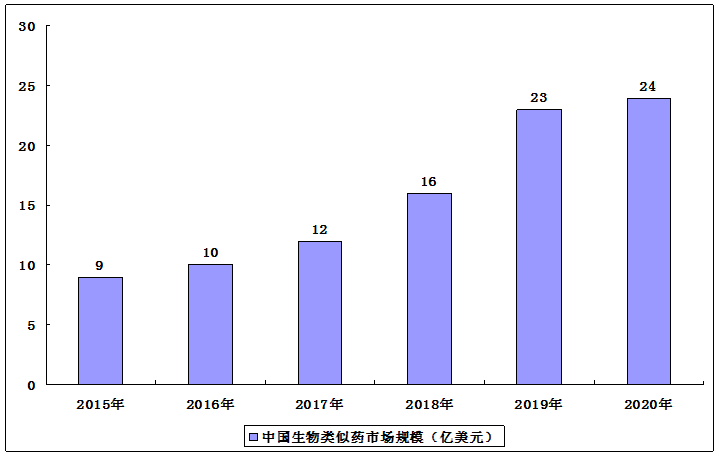
阿达木单抗生物类似药首次获NDA批准
Humira为阿达木单抗的原研药。百奥泰生物制药股份有限公司研制的格乐立在2019年11月自国家药监局获得NDA批件,为中国首个获批的Humira生物类似药。
过去,由于治疗成本高昂,就销售收益而言,中国阿达木单抗市场规模相对较小且增长缓慢。2019年底阿达木单抗获纳入国家医保目录乙类,同时若干Humira生物类似药会陆续获批上市,预计未来中国Humira生物类似药市场规模将较快的速度增长,到2025年市场规模有望达到173亿元
目前,在中国除两种国产Humira生物类似药获批上市外,共有13种Humira生物类似药候选药物正处于临床试验及后期期开发阶段,包括四种处于或完成III期临床阶段及四种正待国家药监局进行NDA审查。
贝伐珠单抗生物类似药市场占比将会增大
安维汀为贝伐珠单抗的原研药。由于推出安维汀生物类似药,原研药安维汀的全球市场规模预期将由2019年的71亿美元减少至2030年的30亿美元,而安维汀生物类似药的全球市场规模预期由2019年的2亿美元增加至2024年的25亿美元,复合年增长率为62.4%。
在中国,首款安维汀生物类似药在2019年12月获批并于2020年开始商业化销售,安维汀生物类似药市场规模预期由2020年人民币7亿元增加至2025年的人民币77亿元,逐渐占中国整体贝伐珠单抗市场的大部份比例。
在中国,目前已有两项安维汀生物类似药获批准。BAT1706为潜在首个正在进行全球III期关键临床试验的本地研发安维汀生物类似药。除BAT1706外,中国有17款安维汀生物类似药候选药物处于临床试验或后期开发阶段,其中四种正待国家药监局进行NDA审查,并有十种处于III期临床试验。
本公司出品的研究报告首先介绍了中国生物类似药行行业市场发展环境、生物类似药行行业整体运行态势等,接着分析了中国生物类似药行行业市场运行的现状,然后介绍了生物类似药行行业市场竞争格局。随后,报告对生物类似药行行业做了重点企业经营状况分析,最后分析了中国生物类似药行行业发展趋势与投资预测。您若想对生物类似药行行业产业有个系统的了解或者想投资中国生物类似药行行业,本报告是您不可或缺的重要工具。
本研究报告数据主要采用国家统计数据,海关总署,问卷调查数据,商务部采集数据等生物类似药行。其中宏观经济数据主要来自国家统计局,部分行业统计数据主要来自国家统计局及市场调研数据,企业数据主要来自于国统计局规模企业统计生物类似药行及证券交易所等,价格数据主要来自于各类市场监测生物类似药行业。
报告目录
2021-2025年中国生物类似药行业发展趋势及供需格局预测报告
第一章 生物类似药行业基本概述
第二章 2019-2021年生物类似药发展环境分析
2.1 宏观经济环境
2.1.1 宏观经济概况
2.1.2 固定资产投资
2.1.3 宏观经济展望
2.2 政策环境
2.2.1 生物类似药相关政策
2.2.2 生物类似药指导原则
2.2.3 生物类似药评价新规
2.2.4 生物类似药对照药政策
2.2.5 国内外生物类似药政策对比
2.3 社会环境
2.3.1 居民收入水平
2.3.2 居民消费水平
2.3.3 居民社会保障
2.3.4 人口老龄化问题
第三章 2019-2021年生物制药行业发展分析
3.1 世界生物医药产业发展综述
3.1.1 全球产业发展格局
3.1.2 欧洲产业强国分析
3.1.3 全球行业专利申请
3.1.4 全球产业融资动态
3.2 2019-2021年全球生物药市场分析
3.2.1 生物药市场规模
3.2.2 生物药销售排名
3.2.3 生物药研发管线
3.2.4 生物药研发动态
3.2.5 生物药交易动态
3.3 2019-2021年中国生物医药产业发展分析
3.3.1 产业发展环境
3.3.2 产业发展热点
3.3.3 行业发展规模
3.3.4 产品上市情况
3.3.5 市场竞争态势
3.3.6 产业园区发展
3.3.7 产业投融资状况
3.4 中国生物制药产业的前景趋势
3.4.1 生物制药行业前景广阔
3.4.2 生物制药未来发展趋势
3.4.3 生物制药企业未来方向
第四章 2019-2021年生物类似药行业发展分析
4.1 全球生物类似药市场分析
4.1.1 市场监管环境
4.1.2 市场发展规模
4.1.3 市场价格分析
4.1.4 市场合作分析
4.1.5 产品研发周期
4.1.6 各国研发情况
4.2 欧美生物类似药发展综述
4.2.1 欧盟批准的生物类似药
4.2.2 美国批准的生物类似药
4.2.3 欧美生物类似药企业格局
4.3 中国生物类似药发展综述
4.3.1 市场发展规模
4.3.2 市场竞争激烈
4.3.3 产品获批情况
4.3.4 企业研发进度
4.3.5 产品价格分析
4.3.6 核心竞争力分析
4.4 生物类似药发展问题及对策
4.4.1 风险管理问题
4.4.2 行业发展挑战
4.4.3 临床研究策略
4.4.4 风险管理措施
第五章 2019-2021年单抗及类似药发展分析
5.1 利妥昔单抗及类似药市场分析
5.1.1 行业研发情况
5.1.2 市场发展规模
5.1.3 市场价格分析
5.2 曲妥珠单抗及类似药市场分析
5.2.1 行业研发情况
5.2.2 行业临床试验
5.2.3 市场发展规模
5.3 贝伐珠单抗及类似药市场分析
5.3.1 行业研发情况
5.3.2 市场发展规模
5.3.3 市场竞争格局
5.3.4 市场价格分析
5.4 阿达木单抗及类似药发展情况
5.4.1 行业研发情况
5.4.2 市场发展规模
5.4.3 市场竞争格局
5.5 依那西普及类似药发展情况
5.5.1 市场研发情况
5.5.2 市场发展规模
5.5.3 市场价格分析
5.6 英夫利西单抗及类似药发展情况
5.6.1 行业研发情况
5.6.2 市场发展规模
5.6.3 市场竞争情况
第六章 2019-2021年生物类似药行业产业链结构分析
6.1 生物类似药行业产业链结构
6.1.1 产业链构成环节
6.1.2 产业链参与主体
6.2 生物类似药行业上游产业发展及影响分析
6.2.1 上游产业发展特征分析
6.2.2 上游产业发展现状分析
6.2.3 上游产业竞争状况分析
6.2.4 上游产业典型企业介绍
6.3 生物类似药行业下游产业发展及需求分析
6.3.1 下游产业发展特征分析
6.3.2 下游产业发展现状分析
6.3.3 下游产业竞争状况分析
6.3.4 下游需求对行业的影响
第七章 2019-2021年全球生物类似药重点企业经营分析
7.1 诺华(山德士)
7.1.1 企业发展概况
7.1.2 企业经营状况
7.1.3 生物类似药规模
7.1.4 产品上市情况
7.1.5 产品研发管线
7.2 辉瑞(Hospira)
7.2.1 企业发展概况
7.2.2 企业经营状况
7.2.3 企业布局动态
7.2.4 产品研发管线
7.2.5 产品上市情况
7.3 三星Bioeois
7.3.1 企业发展概况
7.3.2 产品研发管线
7.3.3 企业发展动态
7.4 Celltrion
7.4.1 企业发展概况
7.4.2 企业经营状况
7.4.3 产品研发管线
7.4.4 企业发展动态
7.5 安进
7.5.1 企业发展概况
7.5.2 企业经营状况
7.5.3 产品研发管线
7.5.4 企业发展动态
第八章 2017-2020年中国生物类似药重点企业经营状况
8.1 信达生物
8.1.1 企业发展概况
8.1.2 产品研发情况
8.1.3 2018年企业经营状况分析
8.1.4 2019年企业经营状况分析
8.1.5 2020年企业经营状况分析
8.2 复星医药
8.2.1 企业发展概况
8.2.2 产品研发情况
8.2.3 经营效益分析
8.2.4 业务经营分析
8.2.5 财务状况分析
8.2.6 核心竞争力分析
8.2.7 公司发展战略
8.2.8 未来前景展望
8.3 沃森生物
8.3.1 企业发展概况
8.3.2 经营效益分析
8.3.3 业务经营分析
8.3.4 财务状况分析
8.3.5 核心竞争力分析
8.3.6 公司发展战略
8.3.7 未来前景展望
8.4 康宁杰瑞
8.4.1 企业发展概况
8.4.2 企业研发管线
8.4.3 2019年企业经营状况分析
8.4.4 2020年企业经营状况分析
8.5 齐鲁制药
8.5.1 企业发展概况
8.5.2 企业研发情况
8.5.3 企业发展成果
8.6 亿帆医药公司发展状况
8.6.1 企业发展概况
8.6.2 企业布局分析
8.6.3 经营效益分析
8.6.4 业务经营分析
8.6.5 财务状况分析
8.6.6 核心竞争力分析
8.6.7 公司发展战略
8.6.8 未来前景展望
第九章 中国生物类似药项目投资建设案例分析
9.1 亿帆医药生物类似药项目投资建设案例
9.1.1 项目基本概述
9.1.2 投资价值分析
9.1.3 资金需求测算
9.1.4 实施进度安排
9.1.5 经济效益分析
9.1.6 风险及应对措施
9.2 北京神州细胞生物类似药新药研发项目
9.2.1 项目基本概况
9.2.2 实施主体投资
9.2.3 项目投资价值
9.2.4 项目实施可行性
9.2.5 项目效益分析
9.3 复星医药生物类似药项目(非公开募资)
9.3.1 项目基本概述
9.3.2 项目实施主体
9.3.3 项目投资概算
9.3.4 项目建设必要性
9.3.5 项目投资可行性
9.4 复宏汉霖生物医药产业化基地项目
9.4.1 项目基本介绍
9.4.2 所涉主要药品
9.4.3 资金需求测算
9.4.4 项目建设进展
第十章 生物类似药行业投资机遇及风险预警
10.1 生物类似药投资机遇分析
10.1.1 商业化发展机遇
10.1.2 跨国企业合作机遇
10.1.3 集中带量采购机遇
10.1.4 PD-1生物类似药机遇
10.2 生物类似药进入壁垒分析
10.2.1 政策壁垒
10.2.2 技术壁垒
10.2.3 资金壁垒
10.3 生物类似药投资风险分析
10.3.1 药物筛选风险
10.3.2 临床开发风险
10.3.3 技术迭代风险
第十一章 生物类似药行业前景展望及预测
11.1 生物类似药发展前景展望
11.1.1 行业发展前景
11.1.2 行业发展趋势
11.2 2021-2025年中国生物类似药行业预测分析
图表目录
图表1 各大机构对生物类似药的定义
图表2 2015-2019年国内生产总值及其增长速度
图表3 2015-2019年三次产业增加值占国内生产总值比重
图表4 2015-2019年万元国内生产总值能耗降低率
图表5 2016-2020年国内生产总值及其增长速度
图表6 2016-2020年三次产业增加值占国内生产总值比重
图表7 2019年中国固定资产投资(不含农户)同比增速
图表8 2019年中国固定资产投资(不含农户)主要数据
图表9 2020年三次产业投资占固定资产投资(不含农户)比重
图表10 2020年分行业固定资产投资(不含农户)增长速度
图表11 2020-2021年我国固定资产投资(不含农户)同比增速
图表12 2021年固定资产投资(不含农户)主要数据
图表13 2015-2020年中国生物类似药相关政策
图表14 中国生物类似药临床设计指导原则
图表15 中国及欧美生物类似药相关法律法规
图表16 中国及欧美生物类似药法律法规异同点
图表17 2019年全国居民人均可支配收入平均数与中位数
图表18 2020年居民人均可支配收入平均数与中位数
图表19 2019年全国居民人均消费支出及构成
图表20 2020年居民人均消费支出及构成
图表21 2011-2019年中国65周岁以上人口数量
图表22 2020年全球生物医药产业发明专利排行榜TOP100(一)
图表23 2020年全球生物医药产业发明专利排行榜TOP100(二)
图表24 2020年全球生物医药产业发明专利排行榜TOP100(三)
图表25 2020年全球生物医药产业发明专利排行榜TOP100(四)
图表26 2020年全球生物医药产业发明专利区域分布
图表27 2020全球生物医药并购事件TOP10
图表28 2012-2019年全球生物药销售额及占比
图表29 2018年全球各类生物药销售额占比
图表30 2019年全球药品销售TOP20
图表31 2014-2019生物制药研发管线(按研发阶段分)
图表32 2019生物制药研发管线(按治疗领域分)
图表33 2020年生物药领域政策
图表34 2020年生物药领域政策(续)
图表35 2014-2030年中国生物药市场规模预测
图表36 国内外优质生物药产品密集获批
图表37 2020年上市生物药企业
图表38 2020年生物医药产业园总榜单(一)
图表39 2020年生物医药产业园总榜单(二)
图表40 2020年生物医药产业园总榜单(三)
图表41 各省市已披露生物药领域融资情况
图表42 生物药已披露的各细分领域融资情况
图表43 各国生物类似药评价标准
图表44 2015-2019年全球生物类似药市场规模
图表45 2015-2019年美国生物类似药涉及产品价格变化一览
图表46 全球生物类似药巨头战略合作
图表47 全球生物类似药巨头战略合作(续)
图表48 部分欧洲市场生物类似药产品的研发周期
图表49 2019年各国家/地区生物类似药研发情况对比
图表50 欧美监管机构批准的生物类似药

